
CAR-T (Chimeric Antigen Receptor T-Cell Immunotherapy),即嵌合抗原受体T细胞免疫疗法。该疗法是一种出现了很多年但近几年才被改良使用到临床
CAR-T (Chimeric Antigen Receptor T-Cell Immunotherapy),即嵌合抗原受体T细胞免疫疗法。该疗法是一种出现了很多年但近几年才被改良使用到临床中的新型细胞疗法。在急性白血病和非霍奇金淋巴瘤的治疗上有着显著的疗效,被 认为是最有前景的肿瘤治疗方式之一。正如所有的技术一样,CAR-T技术也经历一个漫长的演化过程,正是在这一系列的演化过程中,CAR-T技术逐渐走向成熟。
这种新的治疗策略的关键之处在于识别靶细胞的被称作嵌合抗原受体(chimeric antigen receptor, CAR)的人工受体,而且在经过基因修饰后,病人T细胞能够表达这种CAR。在人体临床试验中,科学家们通过一种类似透析的过程提取出病人体内的一些T细胞,然后在实 验室对它们进行基因修饰,将编码这种CAR的基因导入,这样这些T细胞就能够表达这种新的受体。这些经过基因修饰的T细胞在实验室进行增殖,随后将它们灌注回病人体内。这些T细胞利用它们表达的CAR受体结合到靶细胞表面上的分子,而这种结合触发一种内部信号产 生,接着这种内部信号如此强效地激活这些T细胞以至于它们快速地摧毁靶细胞。
近年来,CAR-T免疫疗法除了被用来治疗急性白血病和非霍奇金淋巴瘤之外,经改进后,也被用来治疗实体瘤、自身免疫疾病、HIV感染和心脏病等疾病,具有更广阔的应用空间。基于此,针对CAR-T 细胞疗法取得的最新进展,小编进行一番盘点,以飨读者。
1.Lancet:利用CAR-T细胞成功治疗第二种自身免疫性疾病
doi:10.1016/S0140-6736(23)00023-5
在一项新的研究中,来自德国埃尔朗根大学附属医院的研究人员在世界上首次使用CAR-T细胞成功治疗一名患有严重肌肉炎症(肌炎)的患者(S先生)。这种疾病是由免疫系统的故障引发的,导致肌肉炎症,而且发展为非常严重的疾病的风险很高。相关研究结果于2023年2月15日在线发表在Lancet期刊上,论文标题为“CD19-targeted CAR T cells in refractory antisynthetase syndrome”。
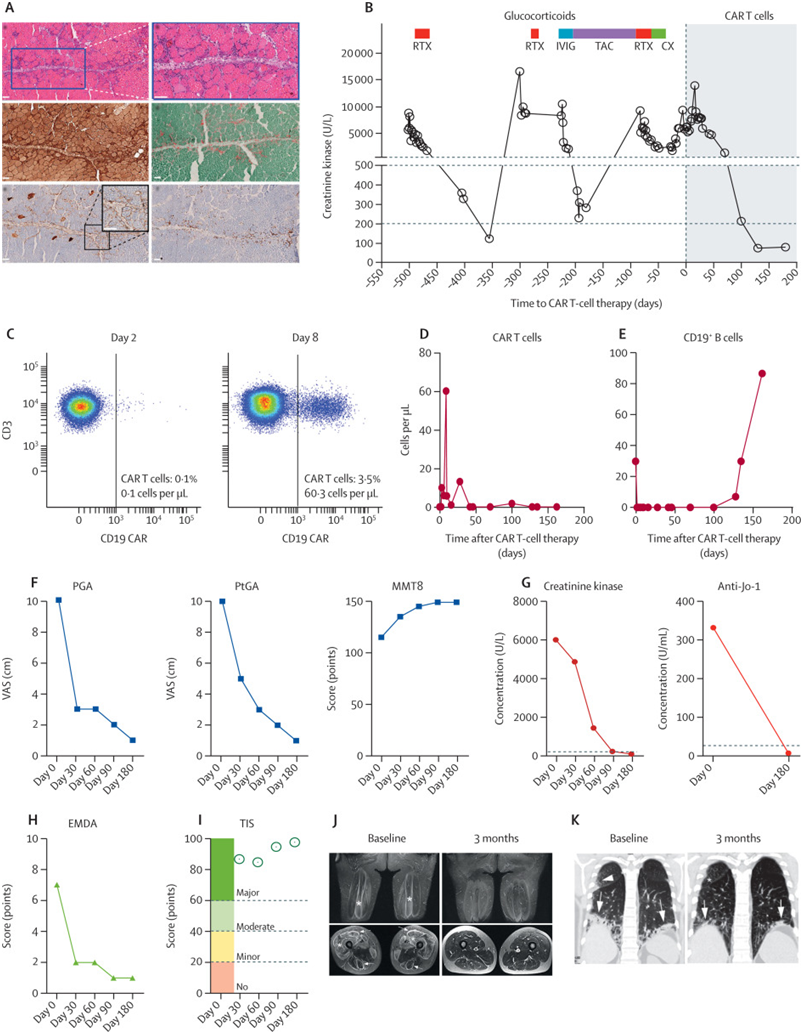
CAR-T细胞对抗合成酶抗体综合征表现的影响。图片来自Lancet, 2023, doi:10.1016/S0140-6736(23)00023-5。
当41岁的S先生去年注意到他得健康状况急剧恶化时,他最初将其归结为病毒感染。然而,当他的健康状况急剧恶化时,他突然不能再移动超过几英尺,而且几乎无法站起来。他的症状是由一种影响他的肌肉、关节、皮肤和肺部的严重自身免疫性疾病---属于抗免疫性肌肉炎症---引起的。他得诊断结果是抗合成酶抗体综合征(anti-synthetase syndrome)。
就S先生而言,所有用于抑制免疫系统的传统疗法都失败了。他被CAR-T细胞疗法所拯救。埃尔朗根大学附属医院的Andreas Mackensen教授解释说,“CAR-T细胞是对从患者血液中提取的T细胞进行基因改造,使之携带识别靶细胞抗原CD19的携带嵌合抗原受体(CAR)。一旦将CAR-T细胞给送回到患者体内,CAR就能让这些经过基因改造的T细胞特异性靶向引发这种疾病的细胞。”
在接受CAR-T细胞输注后,S先生的健康状况有了极大的改善:他的肌肉、肺部和关节的炎症几乎完全消失了。他的力量、表现和耐力都恢复了。论文第一作者Fabian Müller 博士说,“特别令人惊讶的是,S先生能够停止服用所有的免疫抑制药物,特别是皮质类固醇,而且这种疾病却没有再次复发。”在接受CAR-T细胞治疗的六个月后,S先生已从这种自身免疫性疾病中完全康复了。
2.两篇论文表明异体CAR-T细胞有望治疗B-ALL白血病
doi:10.1016/S2352-3026(22)00245-9; doi:10.1158/2767-9764.CRC-22-0175
2016年在英国伦敦大学国王学院启动的CALM临床试验,旨在评估UCART19的治疗潜力,其中-- UCART19是第一种“现成的”CAR-T细胞产品,用于治疗B-ALL成年患者。这项多中心临床试验在英国、美国和日本进行,而且大部分转化研究由伦敦大学国王学院癌症与制药学院雷恩研究所的细胞免疫治疗小组进行。这项研究的最终结果近期发表在Lancet Haematology期刊和Cancer Research Communications期刊上,并建立在2020年发表在Lancet期刊上的初步数据(Lancet, 2020, doi:10.1016/S0140-6736(20)32334-5)之上。
共有25名患有复发性或治疗抵抗性B-ALL的成年患者,他们没有其他治疗选择,之前已接受了化疗药物氟达拉滨(fludarabine)和环磷酰胺(cyclophosphamide)的治疗,其中一些人还接受了一种名为阿仑单抗(alemtuzumab)的抗体。然后,所有患者都接受了名为UCART19 的“现成的”CAR-T细胞,并对不良事件和疾病反应进行了跟踪。
UCART19治疗的副作用被认为是可控的,没有意外的并发症。48%的治疗患者获得了完全缓解,平均持续7.4个月。有疾病反应迹象的患者体内的UCART19增殖水平高于无反应者。进一步的分析还发现,阿仑单抗治疗是UCART19增殖和疾病反应的必要条件。
3.Cell Rep Med:通过抑制常规的信号通路或有望改善CAR-T细胞疗法治疗实体瘤的疗效
doi:10.1016/j.xcrm.2023.100917
近日,一篇发表在国际杂志Cell Reports Medicine上题为“CD28-CAR T-cell activation through FYN kinase signaling rather than LCK enhances therapeutic performance”的研究报告中,来自新加坡国立大学等机构的科学家们通过研究表示,通过抑制常规的信号通路或许就有望改善CAR-T细胞在治疗实体瘤上的疗效。
研究者表示,在CAR-T细胞中(CAR-T细胞疗法需要的特定形式的T细胞)存在着诸如CD28的细胞信号蛋白和淋巴细胞特异性蛋白酪氨酸激酶(LCK),细胞信号转导是细胞开启或关闭特定细胞过程和功能的一种特殊过程,其能作为细胞信号通路上的检查点来发挥作用,对于激活细胞来杀灭肿瘤细胞非常重要。为了解决CAR-T细胞疗法疗效和成本的问题,研究人员通过联合研究发现,在携带CD28的CAR-T细胞中,LCK在细胞信号转导过程中是非必要的,当其被干扰时,名为FYN的另一种蛋白就能接管细胞信号。
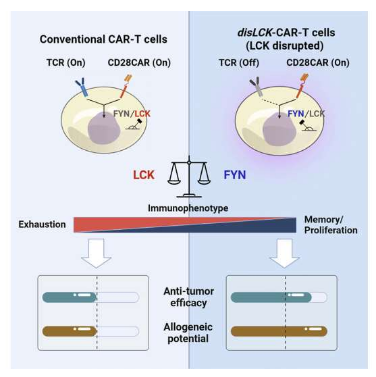
通过抑制常规的信号通路或有望改善CAR-T细胞疗法治疗实体瘤的疗效。图片来源:Cell Reports Medicine (2023). DOI:10.1016/j.xcrm.2023.100917。
而在细胞信号通路中,FYN蛋白是后期的开关之一,然而,由于LCK蛋白在T细胞激活过程中是最主要的开关,在正常的CAR-T细胞中,LCK信号途径通常也是被激活的主要途径,因此当LCK信号被干扰时FYN信号通路就会进行接管。在使用实验室肿瘤模型进行研究时,研究者发现, LCK被干扰的CAR-T细胞会表现出抗肿瘤疗效的增加,而这是FYN信号通路传导的结果,这是因为CAR-T细胞能在体内持续更长时间并会继续杀死肿瘤细胞。
4.Nat Biotechnol:科学家利用一种特殊的分子锚开发出了更加有效的CAR免疫疗法
doi:10.1038/s41587-022-01650-2
在细胞免疫疗法中用于识别癌症的关键蛋白中加入一种分子锚或能使得疗法明显更加有效,近日,一篇发表在国际杂志Nature Biotechnology上题为“Synapse-tuned CARs enhance immune cell anti-tumor activity”的研究报告中,来自美国圣犹大儿童研究医院等机构的科学家们通过研究发现,携带特殊锚定蛋白的免疫细胞或能增加对癌症的杀伤力,无论其细胞类型或靶向作用的癌症类型如何。
分子锚(molecular anchor)概念是一种改善基于嵌合抗原受体(CAR)免疫疗法的新型设计,如今CARs在临床中表现出了一定的研究前景,但尚未在更为广泛的肿瘤类型中取得广泛的成功。研究者Peter Chockley说道,如今我们已经想出了一种新方法来更有效地结合并靶向作用癌细胞。锚定域的设计是模块化的、通用以及跨物种的,我们发现,其能在多种CARs和免疫细胞类型(NK细胞和T细胞)中发挥作用。如今科学家们能通过在人类免疫细胞表面添加工程化的CAR蛋白来对其重编程从而靶向作用癌细胞,CAR-T细胞在临床中治疗特定类型的癌症(比如复发性白血病等)方面展现出了一定的成功,然而,其却并不能成功治疗实体瘤,部分原因是因为免疫细胞激活的相关问题。
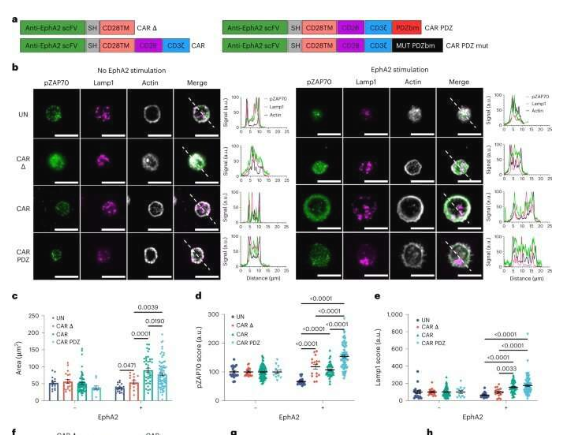
科学家利用一种特殊的分子锚开发出了更加有效的CAR免疫疗法。图片来源:Nature Biotechnology (2023). DOI:10.1038/s41587-022-01650-2。
这项研究中,研究人员发现了一种能在免疫细胞内部锚定CAR分子的新方法,其能促使细胞更容易地被激活,而且相比传统的CARs而言能更加有效地杀灭癌细胞,这种锚定的CARs能增加携带多种肿瘤类型的动物模型的生存率,包括肺癌、骨癌和脑癌等。医学博士Stephen Gottschalk表示,锚定域的发现能很容易地转化为早期的临床检测中,其并不需要任何其它新的技术,我们坚信,这种方法需要在临床中进行测试,因为此前并未有人这样尝试过,而且在临床前研究中其看起来非常有希望。
5.NEJM:临床试验表明CAR-T细胞疗法Ide-cel可用于治疗复发性、难治性多发性骨髓瘤
doi:10.1056/NEJMoa2213614
根据一项新的研究,对于事先经过治疗的复发性、难治性多发性骨髓瘤患者,靶向B细胞成熟抗原(B-cell maturation antigen, BCMA)的嵌合抗原受体(CAR)T细胞(CAR-T)疗法---idecabtagene vicleucel(ide-cel)---能够延长这些患者的无进展生存期,并促进病情缓解。相关研究结果于2023年2月10日在线发表在NEJM期刊上,论文标题为“Ide-cel or Standard Regimens in Relapsed and Refractory Multiple Myeloma”。
在这项新的研究中,西班牙纳瓦拉大学诊所的Paula Rodriguez-Otero博士及其同事们进行了一项国际3期临床试验,涉及复发性、难治性的多发性骨髓瘤成人患者,他们之前接受了2至4种治疗方案,对最后一种治疗方案有抵抗性。共有386名患者被随机分配到ide-cel和五种标准治疗方案中的一种(分别为254和132名患者)。
这些作者发现,在中位随访18.6个月时,ide-cel组和标准治疗方案组的中位无进展生存期分别为13.3和4.4个月(疾病进展或死亡的危险比为0.49)。
在ide-cel组和标准治疗方案组中,分别有71%和42%的患者出现缓解;完全缓解的患者分别为39%和5%。关于总生存期,数据尚不成熟。ide-cel组和标准治疗方案组中分别有93%和75%的患者发生了3级或4级的不良事件。88%接受ide-cel治疗的患者发生了细胞因子释放综合征,15%的患者发生了研究人员确认的神经毒性效应。
6.Nat Commun:在制造过程中对CAR-T细胞进行个性化刺激有望让个性化CAR-T细胞疗法成为现实
doi:10.1038/s41467-023-36126-7
如今,在一项新的研究中,哈佛大学怀斯生物启发工程研究所的David Mooney博士及其团队与丹娜法伯癌症研究所的Catherine Wu博士及其团队证实了在制造过程中对CAR-T细胞进行个性化刺激可以极大地增强所产生的CAR-T细胞产品的一致性和效力。相关研究结果近期发表在Nature Communications期刊上,论文标题为“Enhancing CAR-T cell functionality in a patient-specific manner”。

图片来自Nature Communications, 2023, doi:10.1038/s41467-023-36126-7。
通过使用人工抗原呈递细胞模拟支架(antigen-presenting cell mimicking scaffold, APC-ms),这些作者能够微调T细胞刺激的水平,以匹配从白血病患者那里获得的T细胞的表型,并显著增强它们在体外和体内的肿瘤清除能力。
Mooney说,“我们发现我们表明,由来自癌症患者的T细胞制成的CAR-T细胞产品通常不如来自健康人的CAR-T细胞产品的功能强。利用一种精确可控的密切模拟自然抗原呈递的生物材料方法将CAR-T细胞抗原刺激剂量与患者T细胞的表型相匹配,可以大大改善它们的功能。这种方法可能能进一步实现CAR-T细胞治疗的个性化,并消除目前T细胞制造中存在的不足。”
7.Nat Med:临床试验表明用供体CAR-T细胞有望治疗骨髓瘤患者
doi:10.1038/s41591-022-02182-7
在一项新的研究中,来自美国纽约纪念斯隆-凯特琳癌症中心的研究人员发现捐赠的白细胞可以有效地作为嵌合抗原受体(CAR)T细胞(CAR-T)疗法的一部分来治疗骨髓瘤患者。相关研究结果于2023年1月23日在线发表在Nature Medicine期刊上,论文标题为“Allogeneic BCMA-targeting CAR T cells in relapsed/refractory multiple myeloma: phase 1 UNIVERSAL trial interim results”。
骨髓瘤发生于骨髓中的浆细胞。在这项新的研究中,这些作者给患者提供了不同数量的捐赠的CAR-T细胞,作为骨髓瘤I期临床试验的治疗方案。美国国家卫生研究院的Jennifer Brudno和James Kochenderfer在同期Nature Medicine期刊上发表了一篇标题为“Off-the-shelf CAR T cells for multiple myeloma”的新闻与观点文章,概述了CAR-T细胞疗法的工作原理,并讨论了这项新的研究。

CAR-T细胞浓度按反应分层。图片来自Nature Medicine, 2023, doi:10.1038/s41591-022-02182-7。
这项临床试验涉及向43名要么对其他治疗方法反应不佳要么已经癌症复发的骨髓瘤患者提供不同数量的在体外培养的经过基因改造的T细胞。此外,还对捐赠的T细胞进行了额外的基因改造,以使它们不太可能遭受供者免疫系统的攻击。
每位患者还被给予抗体,以减少免疫系统靶向攻击这些捐赠的T细胞的机会。测试显示,超过一半的志愿者患者(55%)对该疗法有积极反应。该疗法也被认为是安全和可行的。这些作者表示,他们的临床试验是成功的,并计划继续他们的研究工作,以改善结果。
8.Nat Commun:识别出驱动T细胞耗竭的关键基因 或有望帮助开发出更有效的抗癌免疫疗法
doi:10.1038/s41467-022-35583-w
一场艰苦的战斗需要耐力,白细胞在对抗癌症时也是如此,或者更具体地讲,T细胞(或T淋巴细胞)是参与机体免疫系统抵御癌细胞的重要白细胞,然而在这场战斗中T细胞可能会被耗竭并变得疲惫不堪。近日,一篇发表在国际杂志Nature Communications上题为“Deletion of SNX9 alleviates CD8 T cell exhaustion for effective cellular cancer immunotherapy”的研究报告中,来自巴塞尔大学等机构的科学家们通过研究识别出了一种特殊基因,其似乎会促进T细胞的耗竭。
T淋巴细胞的耗竭是20多年来科学家们一直面临的一大研究难题,当长期暴露于肿瘤细胞后,T细胞就会进入到一种耗竭的状态并变得不再那么有效,尽管其能帮助识别有害的肿瘤细胞,但却不会产生很多的物质来消除肿瘤细胞,此外,T细胞也不再会发育为记忆T细胞,后者对于支持宿主机体的免疫反应至关重要。
研究人员利用CRISPR/Cas9技术逐一灭活基因病分析了多种基因的功能,这或许就能帮助他们识别出调节T细胞耗竭的特殊基因,当名为SNX9的基因处于失活状态时,T细胞仍然会保持功能,即使其在肿瘤附近的时间更长。研究者Marcel Trefny说道,SNX9基因似乎会增加短期的机体免疫反应,这在每个小时都能解决疾病的情况下或许被证明是非常重要的,然而在实验中,抑制SNX9基因的功能或能通过减少过度的刺激信号来对免疫细胞的活性进行更为精确地调整,因此,T细胞的活性或许就会在更长的时间内得到保持。研究者还发现,T细胞在发挥功能后并不是简单地死亡,而是频繁地发育为记忆T细胞,该基因所扮演的关键角色或为后期科学家们开发更为有效的免疫疗法开辟新的路径。(生物谷 Bioon.com)
文章来源于生物谷 Bioon.com,如涉及侵权,请24小时内联系我们,我们将马上删除。